蛋白结构模拟物化合物库
在人类蛋白质组中,已鉴定出超过25万种蛋白质-蛋白质相互作用(PPIs)。尽管其中许多相互作用呈现拓扑结构复杂且表面区域庞大的特点,但在许多情况下,成功的结合是通过有限的几个关键残基(“热点”)实现的。文献中有多篇报道描述了通过计算方法和多样性导向策略开发PPIs的小分子调节剂。其中,非肽类α-螺旋和β-转角模拟物因其在癌症、神经退行性疾病、炎症和免疫系统疾病等多种失调通路中的关键作用而尤为重要。
蛋白质模拟库包含8960个化合物。
https://enamine.net/compound-libraries/targeted-libraries/ppi-library/protein-mimetics-library
- 陶术生物的所有产品和服务仅用于科学研究,我们不为任何个人用途提供产品和服务。

- 规格
- 1 mg
- 100 μL x 10 mM (in DMSO)
- 250 μL x 10 mM (in DMSO)
技术资料
- 产品描述:
库设计
传统的三残基方法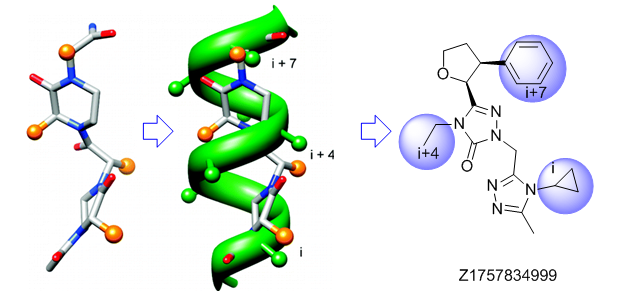 α-螺旋模拟物
α-螺旋模拟物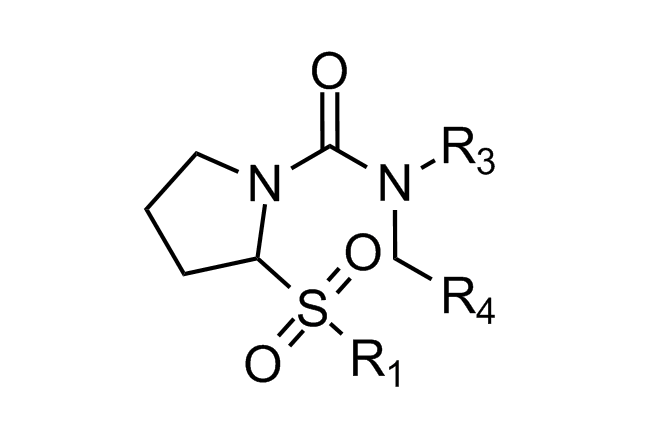 β-转角模拟物
β-转角模拟物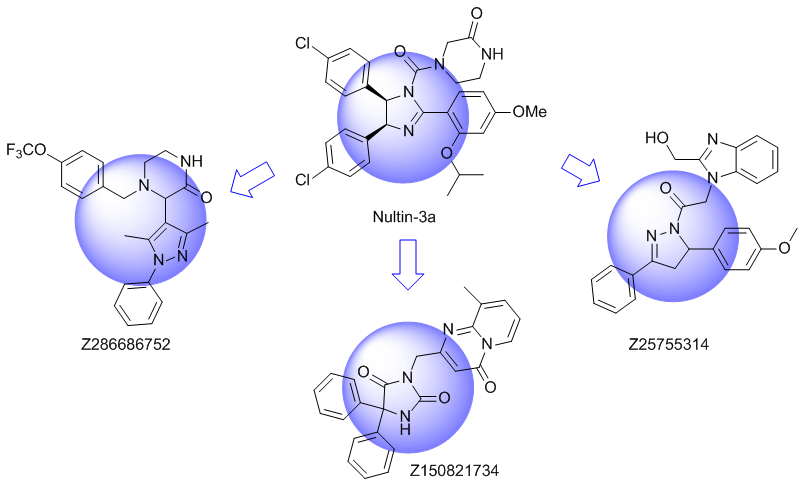 基于配体的方法
基于配体的方法基于靶标的设计方法:我们针对选定的α-螺旋结构域和β-转角(如MDM2-p53、MDM2-CK1α、HIF1-α、MEF2-HDAC4、HIV-1 gp41、CD81/CV、Bcl-2/Bcl-xL等)进行了聚焦化合物库的设计。通过虚拟筛选后,优先选择了具有新颖化学型(新母核)的分子结构。
在“传统”的三残基模拟策略中,我们设计了具有非常规核心结构的化合物,这些核心携带规则的关键残基,能够模拟位于同一识别面(“热点”)上的i、i+3/i+4及i+7位残基。在模拟α-螺旋界面时,我们也考虑了双面螺旋模拟物。对于β-转角模拟物,我们应用了三种基于不同相互作用类型的查询模型:π-π堆积、阳离子-π相互作用与氢键相互作用,以及S-π相互作用。后续的聚焦设计工作,以模拟Bim BH3结构域与Mcl-1和Bcl-2之间的相互作用为例,鉴定出了具有高Fsp3(sp3杂化碳原子比例)特征的稠合多氢化氮杂环化合物。
基于配体的设计方法:我们筛选了与已知α-螺旋和β-转角模拟物拓扑结构相近的新化学型。基于形状的相似性筛选和药效团筛选是库设计的主要工具。
我们特别筛选了具有阶梯状环状骨架、富含Fsp3的独特优势骨架,以增强与靶标α-螺旋和β-转角基序的拓扑及药效团相互作用。分子特征
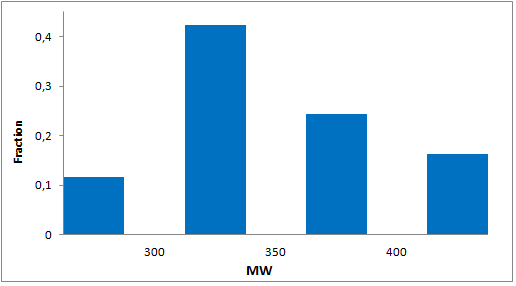
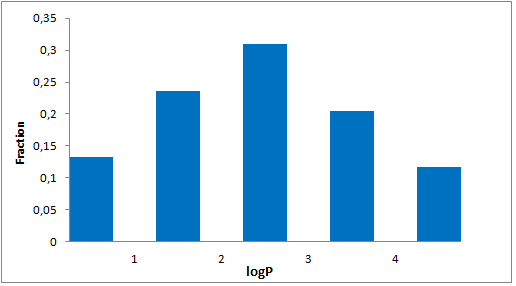
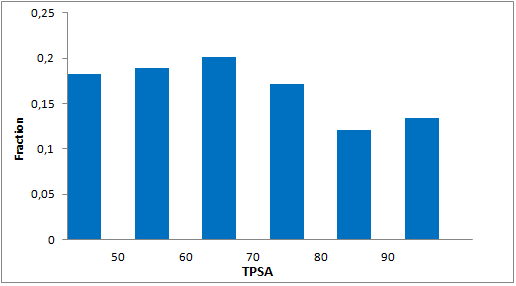
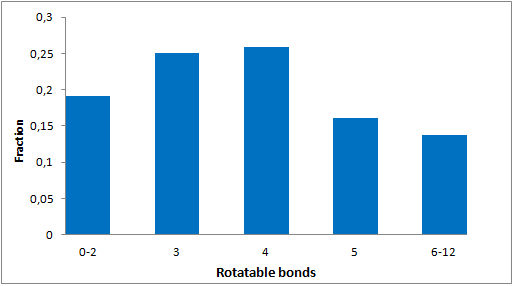
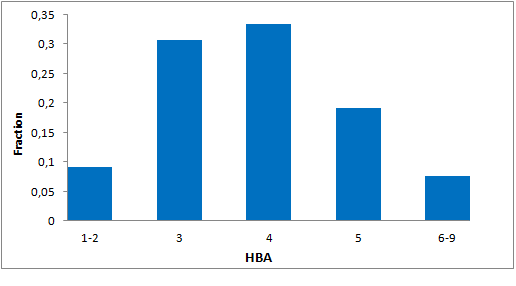
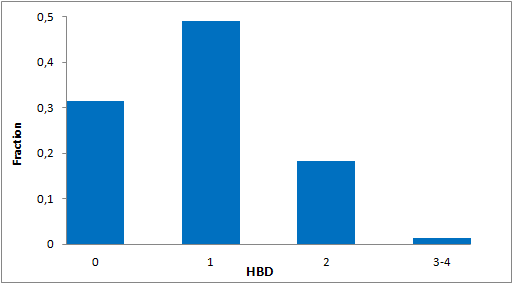
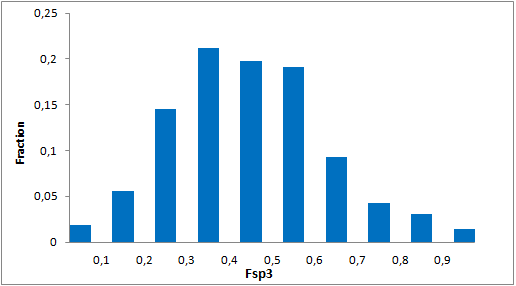
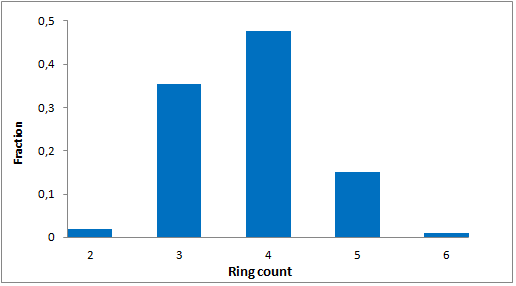
- 包装和储存:
- 可选用DMSO耐受的96/384孔板或2D 条形码编码管;
- 干粉蓝冰运输,DMSO溶液干冰运输;
- 排布:96孔板:1st & 12th 空白对照,384孔板:1st & 2nd & 23th & 24th空白对照。
寻找合适的化合物库

 陶术生物化合物库目录 (78 MB)
陶术生物化合物库目录 (78 MB)  库化合物信息
库化合物信息 Excel
Excel